EUDAMED Zaman Çizelgesi – Temmuz 2025 Güncellemesi
Avrupa Komisyonu tarafından yayınlanan 2025 EUDAMED zaman çizelgesi ile tıbbi cihaz ve IVD sektöründeki tüm paydaşlar için yeni kilometre taşları ve son tarihler açıklandı. Bu güncelleme, üreticiler, distribütörler ve onaylanmış kuruluşlar için EUDAMED’e geçişte kritik adımları ve zorunlu kullanım tarihlerini içeriyor.
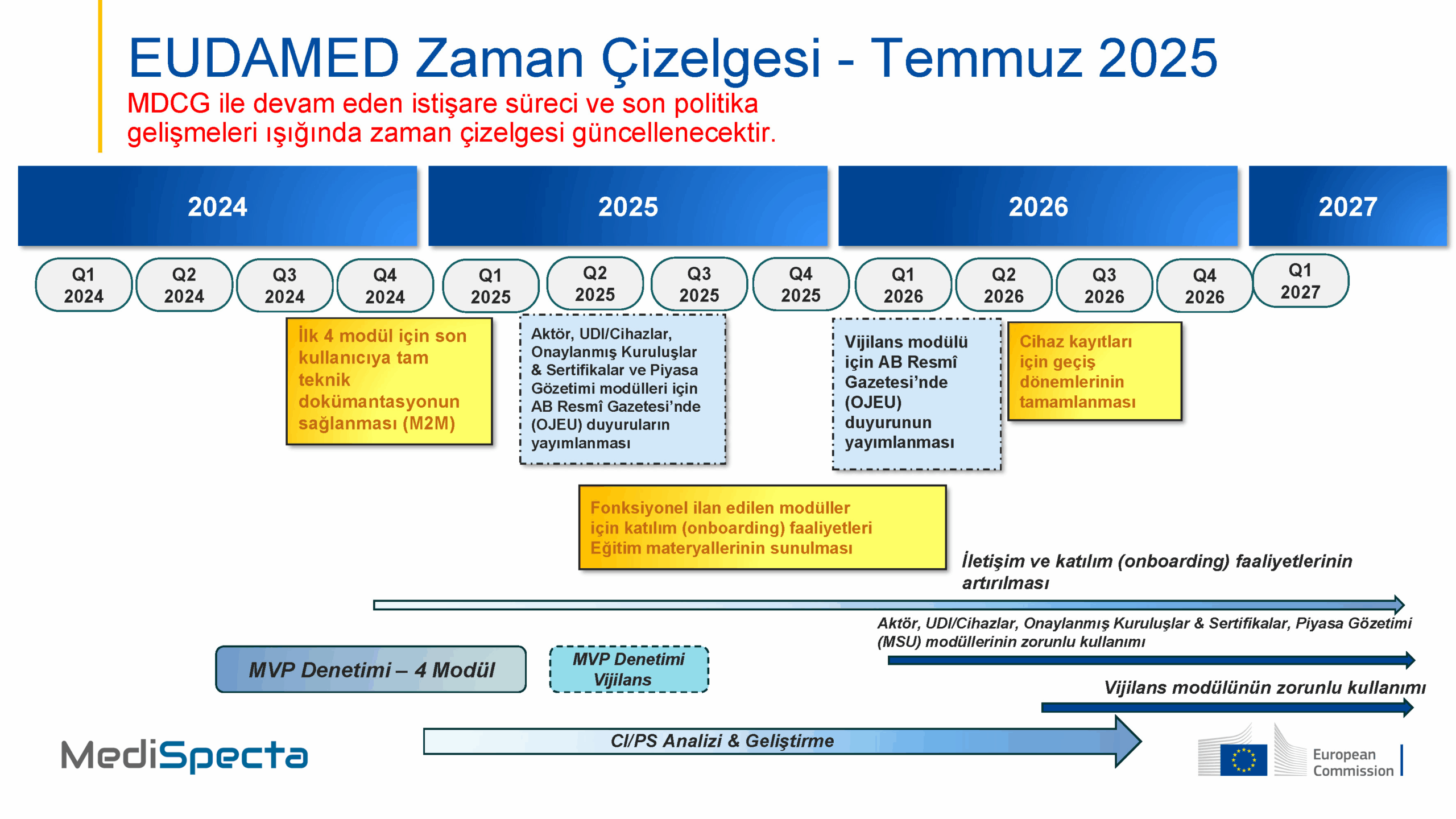
EUDAMED Yol Haritasında Öne Çıkan Başlıklar
- 2024: İlk 4 modül için son kullanıcıya tam teknik dokümantasyonun sağlanması (M2M).
- 2025: Aktör, UDI/Cihazlar, Onaylanmış Kuruluşlar & Sertifikalar ve Piyasa Gözetimi modülleri için AB Resmî Gazetesi’nde (OJEU) duyuruların yayımlanması.
- 2025: Fonksiyonel ilan edilen modüller için katılım (onboarding) faaliyetleri ve eğitim materyallerinin sunulması.
- 2026: Vijilans modülü için AB Resmî Gazetesi’nde duyurunun yayımlanması, cihaz kayıtları için geçiş dönemlerinin tamamlanması.
- 2026 ve sonrası: Tüm ana modüllerin ve Vijilans modülünün zorunlu kullanımı.
2025 Temmuz güncellemesi ile EUDAMED platformunun tam devreye alınmasına ilişkin takvim revize edildi. MDCG istişareleri ve son AB politika gelişmeleri doğrultusunda, sektör oyuncularının teknik dokümantasyon, onboarding ve zorunlu modül kullanımı gibi başlıklarda yeni yükümlülükleri bulunuyor.
EUDAMED nedir? EUDAMED (European Database on Medical Devices), tıbbi cihazlar ve IVD’ler için AB genelinde şeffaflığı, izlenebilirliği ve denetimi artırmayı hedefleyen bir veri tabanıdır. Platformun devreye alınması, hem regülasyonlara (MDR/IVDR) hem de pazar erişimine uyum açısından kritik önemdedir.
Takvimdeki kritik tarihleri ve modül gerekliliklerini kaçırmamak için Avrupa Komisyonu ve MDCG’nin resmi duyurularını düzenli olarak takip etmek gerekmektedir.
EUDAMED platformu neden zorunlu hale geliyor?
Zaman çizelgesindeki “M2M” ne anlama geliyor?
Onaylanmış Kuruluşlar ve üreticiler için kritik tarihler hangileri?
Vijilans modülünün devreye girmesi ne zaman?
Geçiş dönemini kaçırırsam ne olur?
Daha fazla bilgi ve güncel gelişmeler için:
- Avrupa Komisyonu Resmi EUDAMED sayfası: EUDAMED
- MDCG resmi duyuruları: MDCG Guidance


