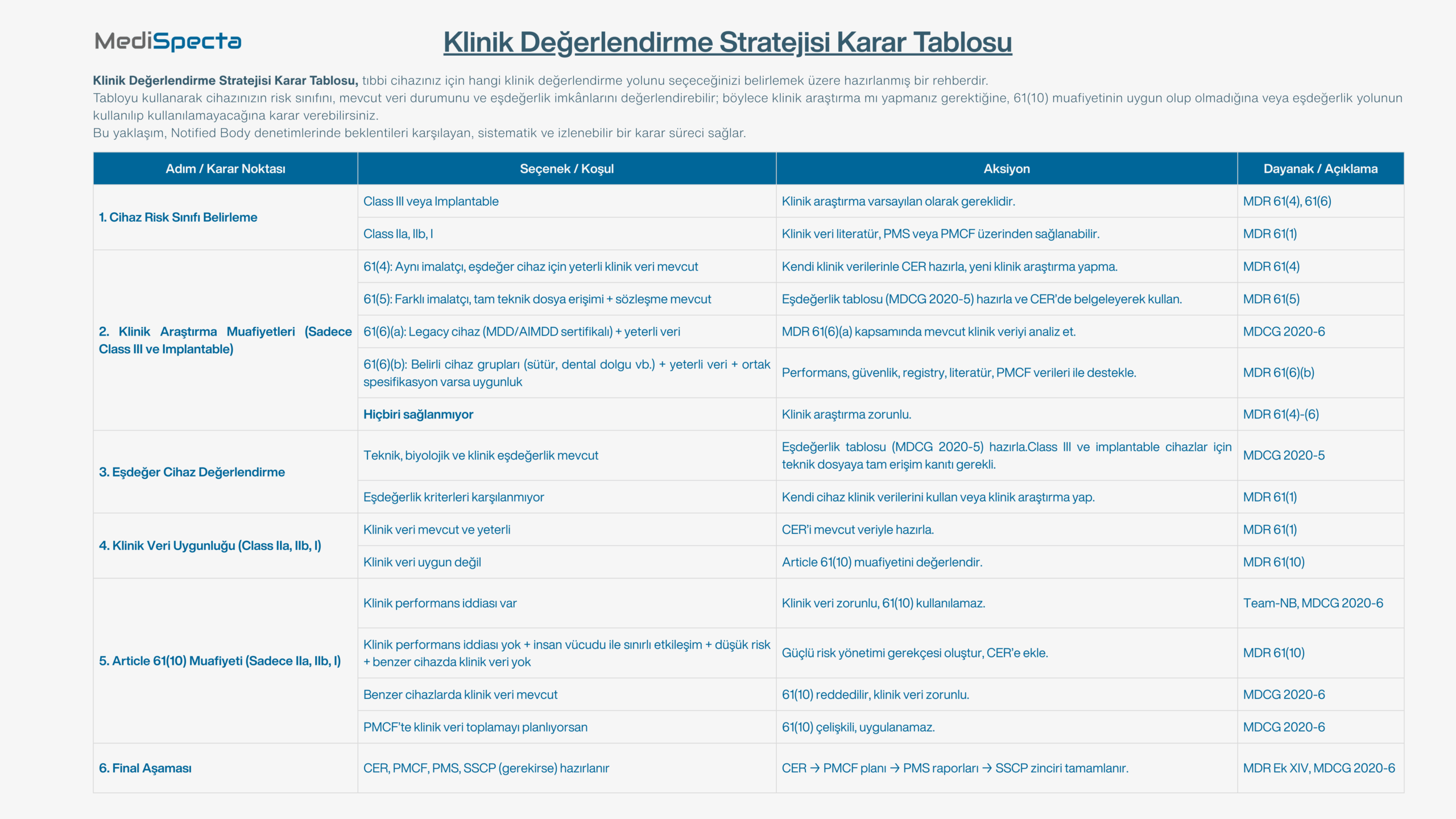
Klinik Değerlendirme Stratejisi Karar Tablosu
MDR (2017/745) kapsamında cihazınız için doğru klinik değerlendirme yolunu seçmek kritik bir adımdır. Bu tablo sayesinde cihazınızın risk sınıfını, mevcut veri durumunu ve eşdeğerlik imkânlarını değerlendirebilirsiniz.
Böylece aşağıdaki sorulara net yanıt bulabilirsiniz:
- Klinik araştırma yapmam gerekiyor mu?
- 61(10) muafiyeti benim cihazım için geçerli mi?
- Eşdeğerlik yolu kullanılabilir mi?
Bu yaklaşım, Notified Body denetimlerinde beklentileri karşılayan, sistematik ve izlenebilir bir karar süreci oluşturmanıza yardımcı olur.
Adım 1: Risk Sınıfı Belirleme
İlk olarak cihazınızın doğru risk sınıfı belirlenmelidir. Yanlış sınıflandırma tüm sürecin hatalı ilerlemesine neden olabilir.
- Class III veya Implantable: Genellikle klinik araştırma varsayımıyla başlanır.
- Class IIa, IIb, I: Mevcut klinik veri ve PMS/PMCF verileri yeterliyse klinik araştırma gerekmeden CER hazırlanabilir.
Püf noktası: Risk sınıflandırmasını yanlış yapmak, dosyanızın NB tarafından geri çevrilmesine yol açabilir.
Adım 2: Klinik Araştırma Muafiyetleri
Sadece Class III ve implantable cihazlar için geçerlidir. MDR madde 61’de üç temel muafiyet tanımlanmıştır:
- 61(4): Aynı üretici eşdeğer cihaz + yeterli klinik veri → yeni çalışma gerekmez.
- 61(5): Farklı üretici ama tam teknik dosyaya erişim + sözleşme → eşdeğerlik kabul edilebilir. (MDCG 2020-5)
- 61(6): Legacy cihazlar veya belirli cihaz grupları (ör. sütür, dental dolgu) için yeterli veri ve ortak spesifikasyon varsa → klinik araştırma gerekmez. (MDCG 2020-6)
Eğer bu koşullar sağlanmıyorsa, klinik araştırma zorunludur.
Adım 3: Eşdeğerlik Değerlendirmesi
Eşdeğerlik, klinik araştırma zorunluluğunu azaltabilir. Ancak Class III ve implantable cihazlarda, üçüncü taraf cihaz için tam teknik dosya erişimi belgelenmelidir.
- Teknik, biyolojik ve klinik eşdeğerlik birlikte gösterilmelidir.
- Erişim kanıtı sözleşme veya resmi belge ile sunulmalıdır.
Püf noktası: Eşdeğerlik kriterleri sağlanmazsa, kendi cihazınıza ait klinik verilerle ilerlemeniz gerekir.
Adım 4: Klinik Veri Yeterliliği
Class IIa, IIb ve I cihazlar için mevcut klinik verilerin yeterliliği değerlendirilir:
- Veri yeterli: Doğrudan CER hazırlanabilir.
- Veri yetersiz: 61(10) muafiyeti değerlendirilir veya PMCF/klinik araştırma planlanır.
Adım 5: 61(10) Muafiyeti
Bu madde, özellikle düşük riskli cihazlar için uygulanabilir. Ancak sıkı kriterleri vardır:
- Klinik performans iddiası olmamalı.
- Düşük riskli ve sınırlı etkileşim olmalı.
- Benzer cihazlarda klinik veri bulunmamalı.
Eğer bu şartlar sağlanmazsa, 61(10) kullanılamaz ve klinik araştırma zorunlu hale gelir.
Adım 6: Final Aşaması
Tüm süreç tamamlandığında aşağıdaki dokümanlar hazırlanır:
- CER (Clinical Evaluation Report)
- PMCF Plan & Rapor
- PMS Raporları
- Gerekirse SSCP (Summary of Safety and Clinical Performance)
Sonuç
Klinik değerlendirme süreci, sadece bir yasal gereklilik değil, aynı zamanda hasta güvenliği ve cihazın piyasadaki başarısı için temel bir süreçtir. Bu tabloyu kullanarak:
- Doğru klinik stratejiyi belirleyebilir,
- Notified Body denetimlerinde güçlü bir pozisyon alabilir,
- İzlenebilir ve sistematik bir süreç yürütebilirsiniz.
Kısacası: Doğru kararlar, başarılı bir CE sürecinin anahtarıdır.