
Tıbbi Cihaz Yönetmeliği Madde 10/A: Yeni Bildirim Yükümlülükleri
Tıbbi Cihaz Yönetmeliği Madde 10/A: Yeni Bildirim Yükümlülükleri (MDR) Tıbbi Cihaz Yönetmeliği Madde 10/A: Yeni Bildirim Yükümlülükleri (MDR) Avrupa[…]
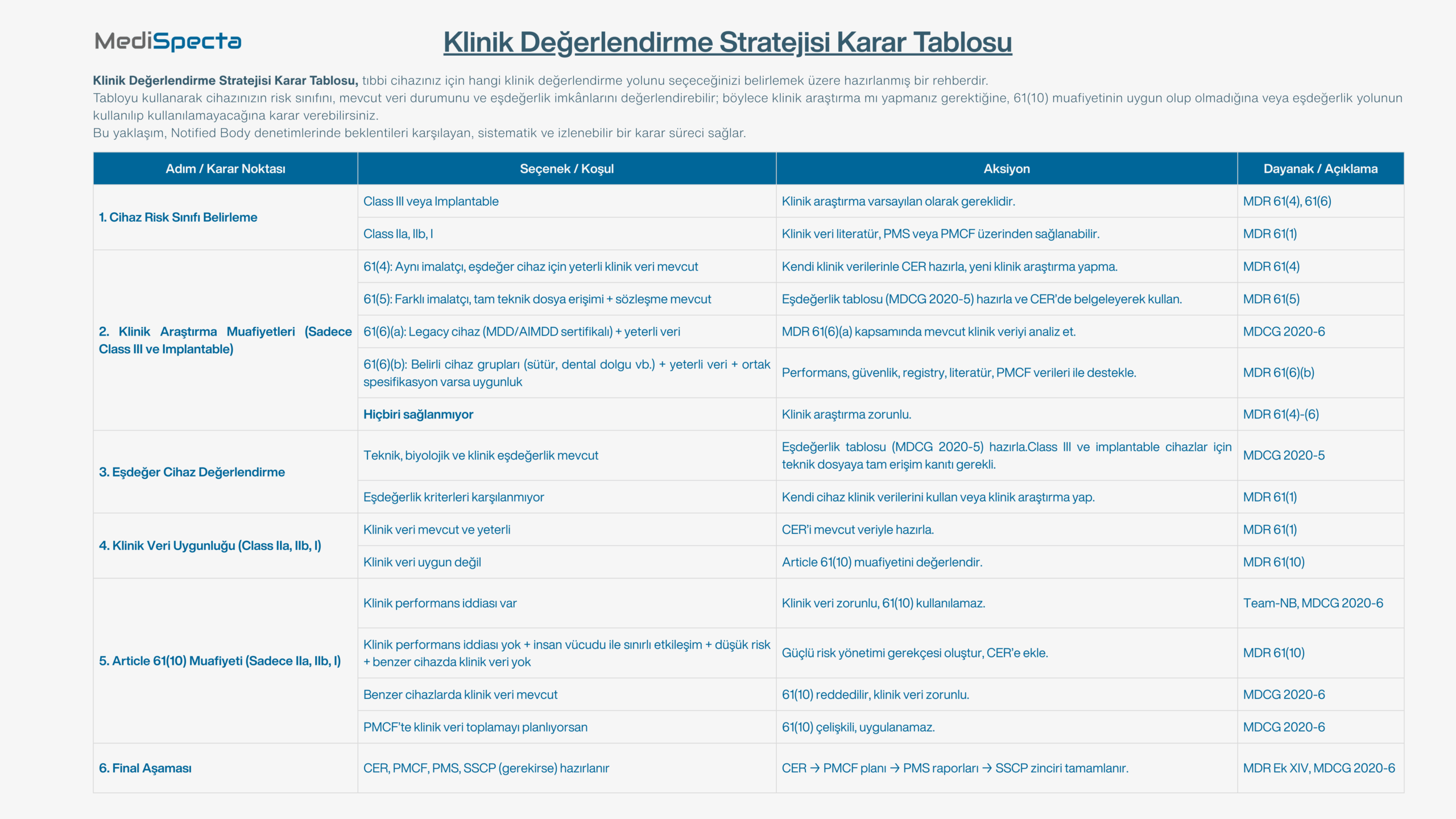
Klinik Değerlendirme Stratejisi Karar Tablosu
Klinik Değerlendirme Stratejisi Karar Tablosu MDR (2017/745) kapsamında cihazınız için doğru klinik değerlendirme yolunu seçmek kritik bir adımdır. Bu[…]

Tıbbi Cihaz Teknik Dosya: Nedir, Nasıl Hazırlanır, Gereklilikleri Nelerdir?
Tıbbi Cihaz Teknik Dosya: Nedir, Nasıl Hazırlanır, Gereklilikleri Nelerdir? Tıbbi cihaz üreticileri için teknik dosya, cihazın güvenliğini, performansını ve[…]

Cihazın DNA’sı, Hasta Güvenliğinin Pusulası: MDR Uyumunda Net Yol Haritası
Cihazın DNA’sı, Hasta Güvenliğinin Pusulası: MDR Uyumunda Net Yol Haritası Bu yayında tıbbi cihazlarda hasta güvenliğinin DNA’sını oluşturan tasarım,[…]

2017/745/EU MDR Sürecinde Yolumuzu Nasıl Buluyoruz?
MDR Sürecinde Yolumuzu Nasıl Buluyoruz? Giriş MDR (2017/745) artık hepimizin gündeminde. Biz Medispecta olarak firmalarla çalışırken aynı tabloyu görüyoruz:[…]

MDR Doğrultusunda Belgelendirilmeyecek Tıbbi Cihazlar ve ÜTS Uygulamaları Hakkında Duyuru
MDR Doğrultusunda Belgelendirilmeyecek Tıbbi Cihazlar ve ÜTS Uygulamaları Hakkında Duyuru Türkiye İlaç ve Tıbbi Cihaz Kurumu (TİTCK), AB MDR[…]

PSUR’da Ürün Kullanım Sıklığı: Gerçek Hayattan Örneklerle
PSUR Kullanım Sıklığı: MDCG 2022-21 Rehberine Göre Açıklama PSUR Kullanım Sıklığı: MDCG 2022-21 Rehberine Göre PSUR (Periodic Safety Update[…]

PSUR Nedir? MDR’ye Göre Periodik Güvenlik Güncelleme Raporu
PSUR Nedir? MDR’ye Göre Periodik Güvenlik Güncelleme Raporu (Kılavuz + Şablon) PSUR Nedir? MDR’ye Göre Periodik Güvenlik Güncelleme Raporu[…]

Tıbbi Cihaz Danışmanlığı Rehberi: CE, ISO 13485, MDR ve FDA
Tıbbi Cihaz Danışmanlığı Rehberi: CE, ISO 13485, MDR ve FDA (2025) Tıbbi Cihaz Danışmanlığı Rehberi: CE, ISO 13485, MDR[…]

Efsane mi? Gerçek mi? – Seri 1
Efsane mi? Gerçek mi? — Tıbbi Cihaz Danışmanlığı Tıbbi Cihaz CE belgelendirme, DÖF/CAPA, risk yönetimi ve etiket/IFU güncellemelerinde sahada[…]

